

オステオノバス株式会社
「腰が痛い」「足が痺れる」などの症状は日常生活の中で時々耳にされることと思います。その原因が脊椎にある場合、一般的にはまず保存療法を行い、それでも痛みや痺れが取れない時には多くの場合手術になります。
例えば「脊柱管狭窄症」。加齢や重労働等によって骨や関節が変形、もしくは椎間板や靭帯が硬く飛び出し、神経やその周りの血行を阻害する症状。60歳以上の高齢者に多く見られる病気です。
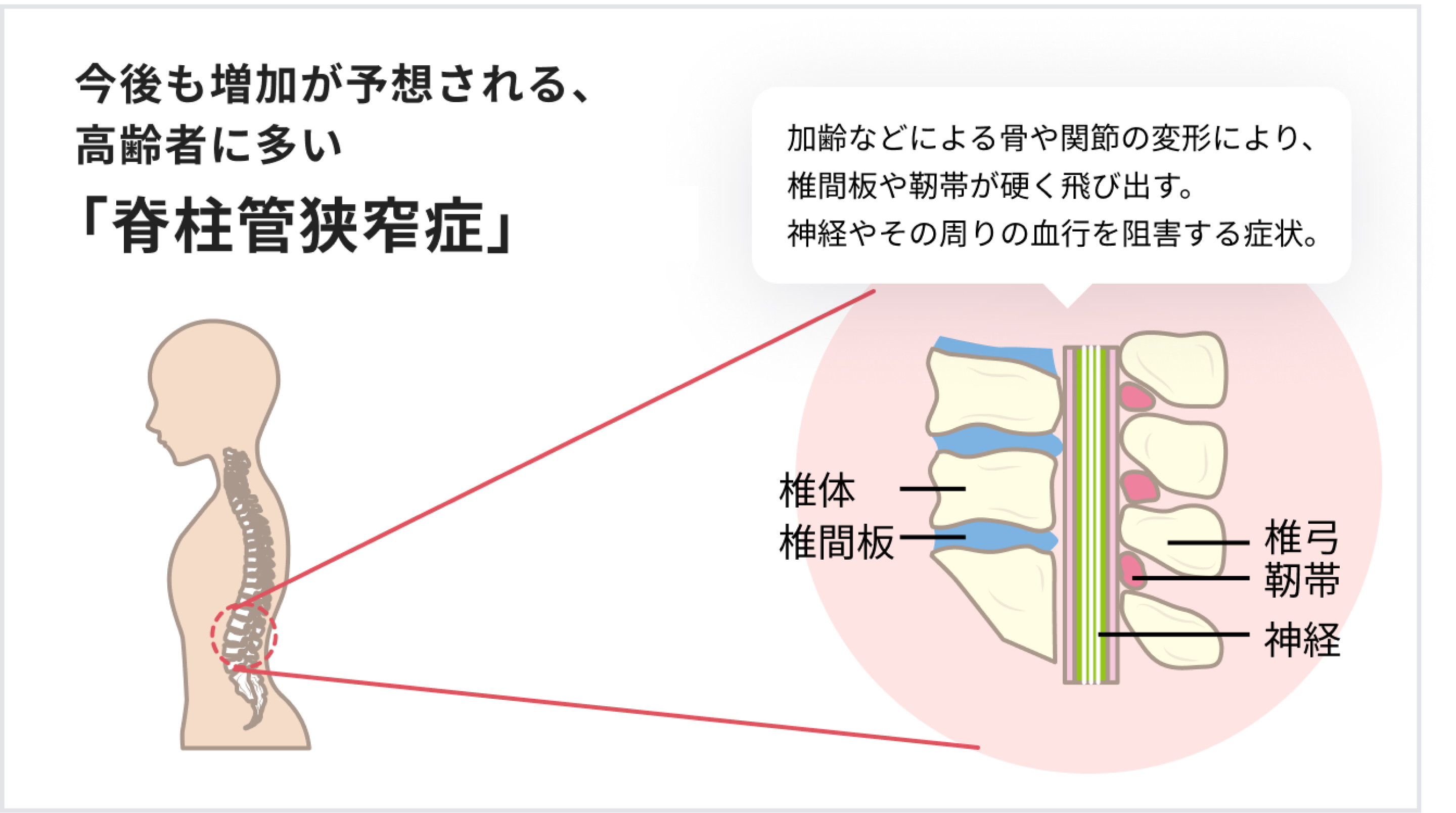
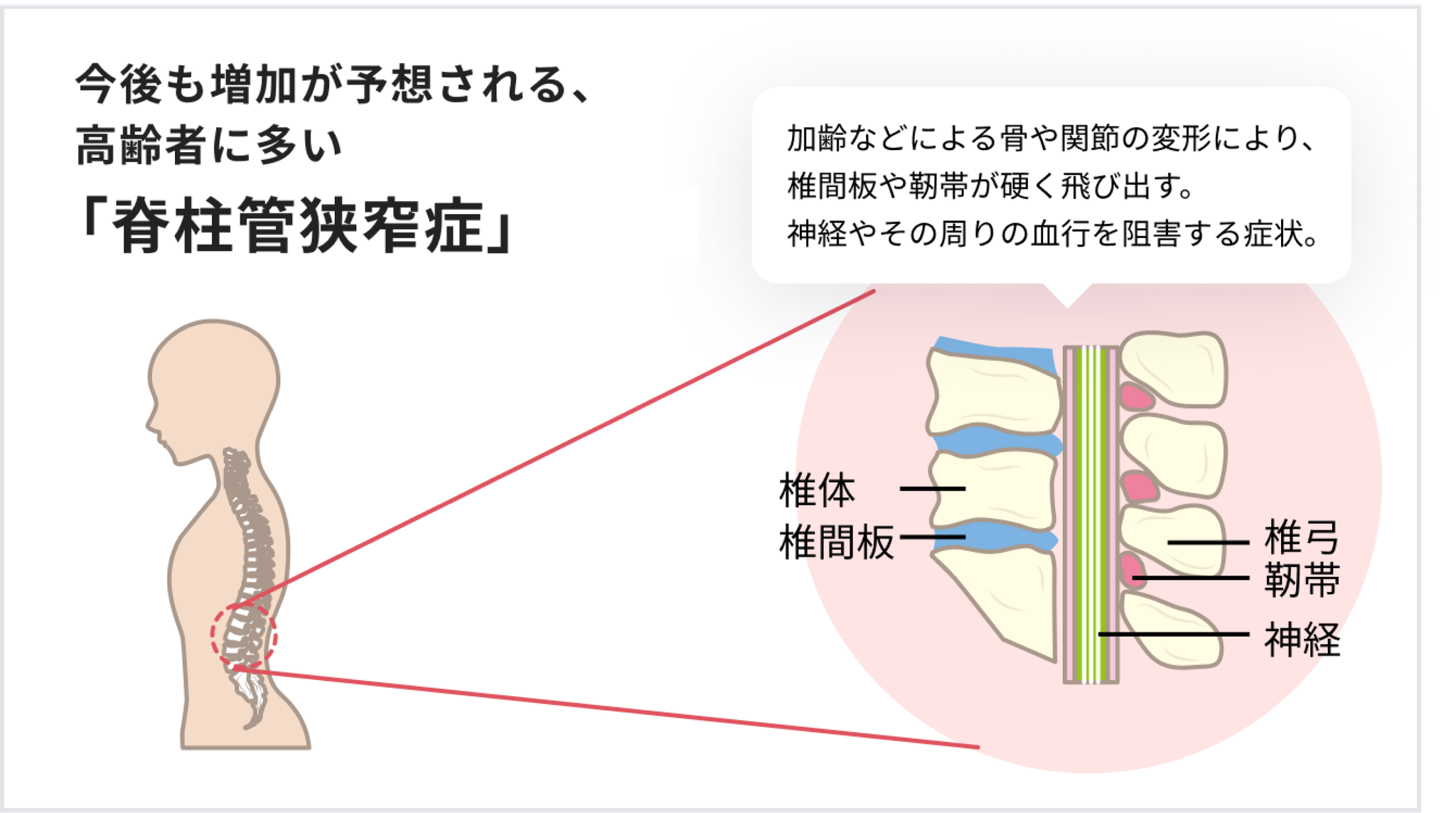
この症状改善のため手術をする場合に、よく選択されるのが椎体間固定術。
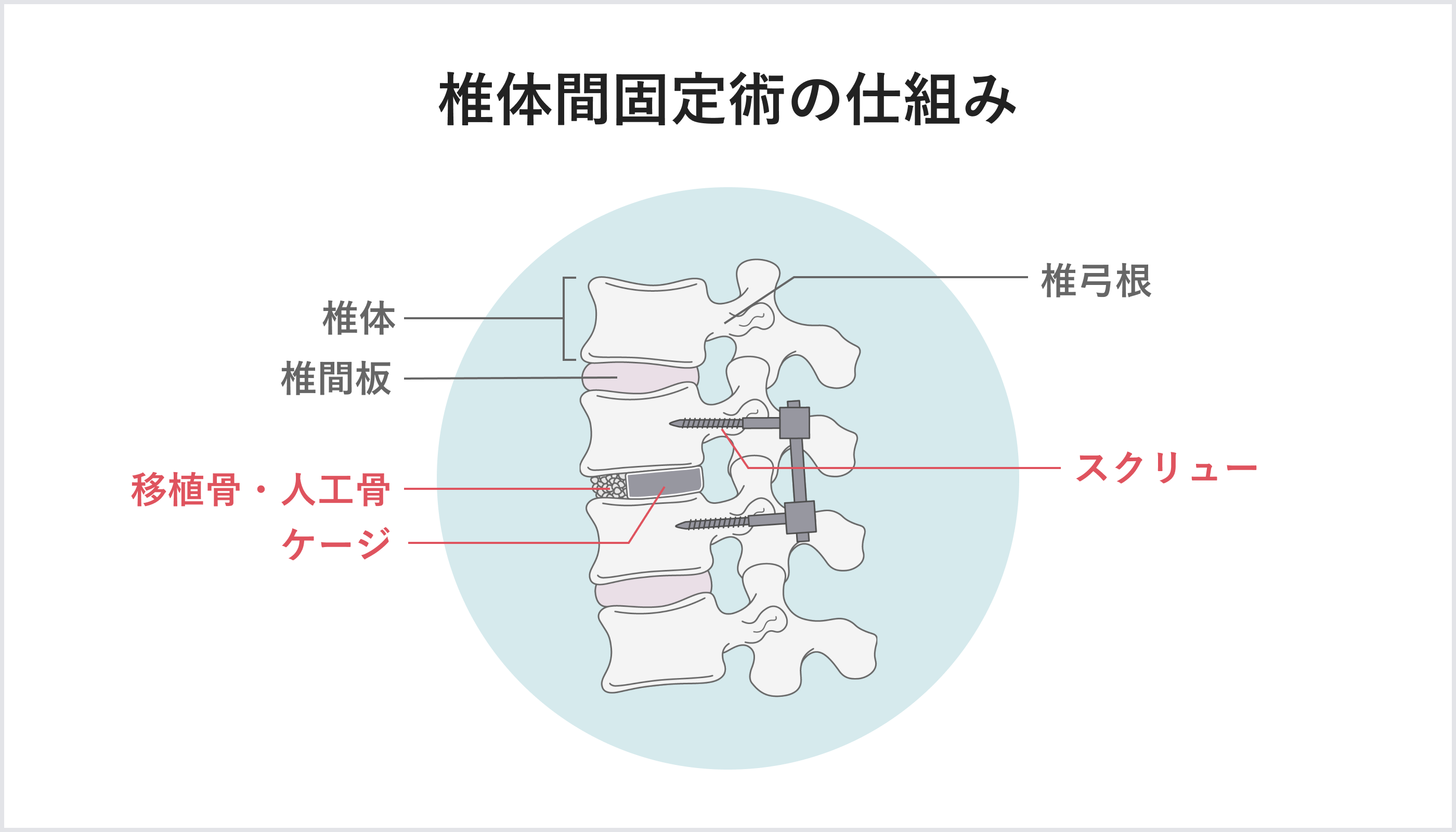
脊椎固定術にも様々な種類がありますが、頻繁に行われているのはケージを使用した椎体間固定術です。椎体と椎体の間のクッションのような役割を果たしている椎間板。椎体間固定術ではこの椎間板を除去し、代わりに支えとなるようケージを挿入します。同時に、スクリューとロッドを装着してサポート。ケージは椎骨よりも小さいため、ケージの周りや内側に人工骨や移植骨を使用し、余っているスペースを埋めていきます。時間と共に椎体やケージの周りに骨が出来ていき、上下にある椎体同士が癒合します。
脊柱管狭窄症の手術は全国の病院で年間約65,173件(2019年)行われています。
様々な人工骨があるなかで、現在主に使われているものとして顆粒状、ブロック状、生物由来(特定生物由来製品)のものがあります。顆粒状のものは術部に置いておけますが、術後患者さんが動かれた時に顆粒が移動してしまう心配があります。またブロック状の場合、骨の形状に合わせて留置するのが難しいという課題があります。手術部位の奥に入れるのも困難です。他にも人の骨を原料に使った特定生物由来製品がありますが、抵抗を感じる患者さんもおられます。

当社の親会社米国OsteoNovus Inc.では、このような医師が感じる不便さや患者さんの心配事を解決すべく、安全で使い勝手の良い製品開発に取り組みました。
親会社であるOsteoNovus Inc.創業者の1人、トレド大学のバドゥーリ(Bhaduri)教授は長年リン酸カルシウムなどのバイオ材料研究に従事してきました。同教授の研究成果を基に開発されたのが「ノボグロ(NovoGro)」というユニークな人工骨です。ネーミングの由来は Novo (新しい)+Grow(成長)を組み合わせた造語です。
「ノボグロ(NovoGro)」は、アメリカで発明界のオスカーとも呼ばれるThe R&D100を受賞。米国「R&D World Magazine」主催の権威ある賞で、世界的研究機関や企業が開発し、過去1年に実用化された製品や技術のうち最も優れた100件を選出するもの。過去にはトヨタ自動車の技術も表彰されています。
当時のトレド大学教授で、当社代表取締役会長(OsteoNovus Inc. 創業者兼CEO)のアガルワル(Agarwal, MD)は、使い勝手を良くする観点から開発に深く関わりました。彼は主に英国で脊椎外科医として数千例の外科手術を行っており、製品開発では医師としての要望をとことん追求しました。

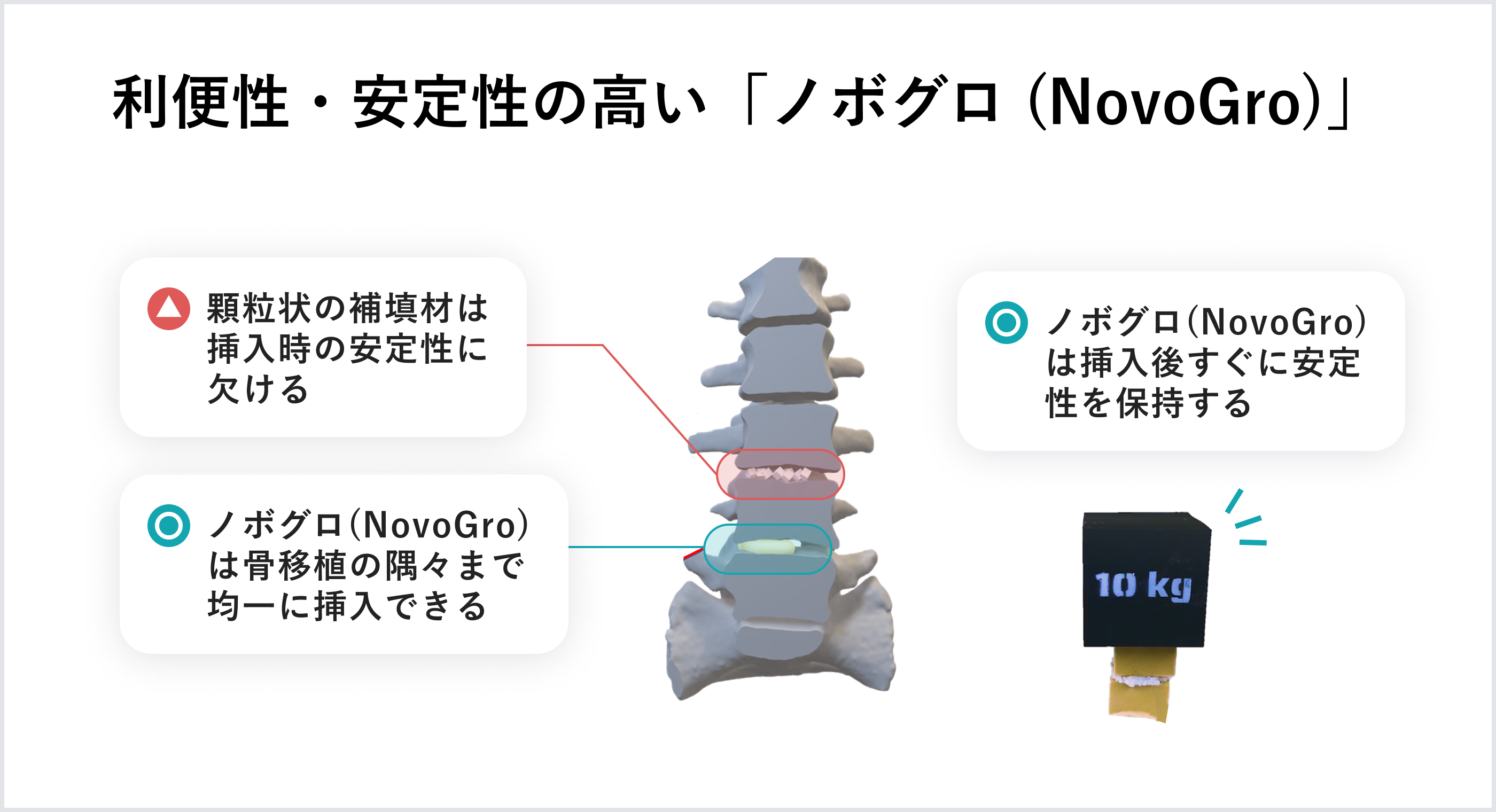
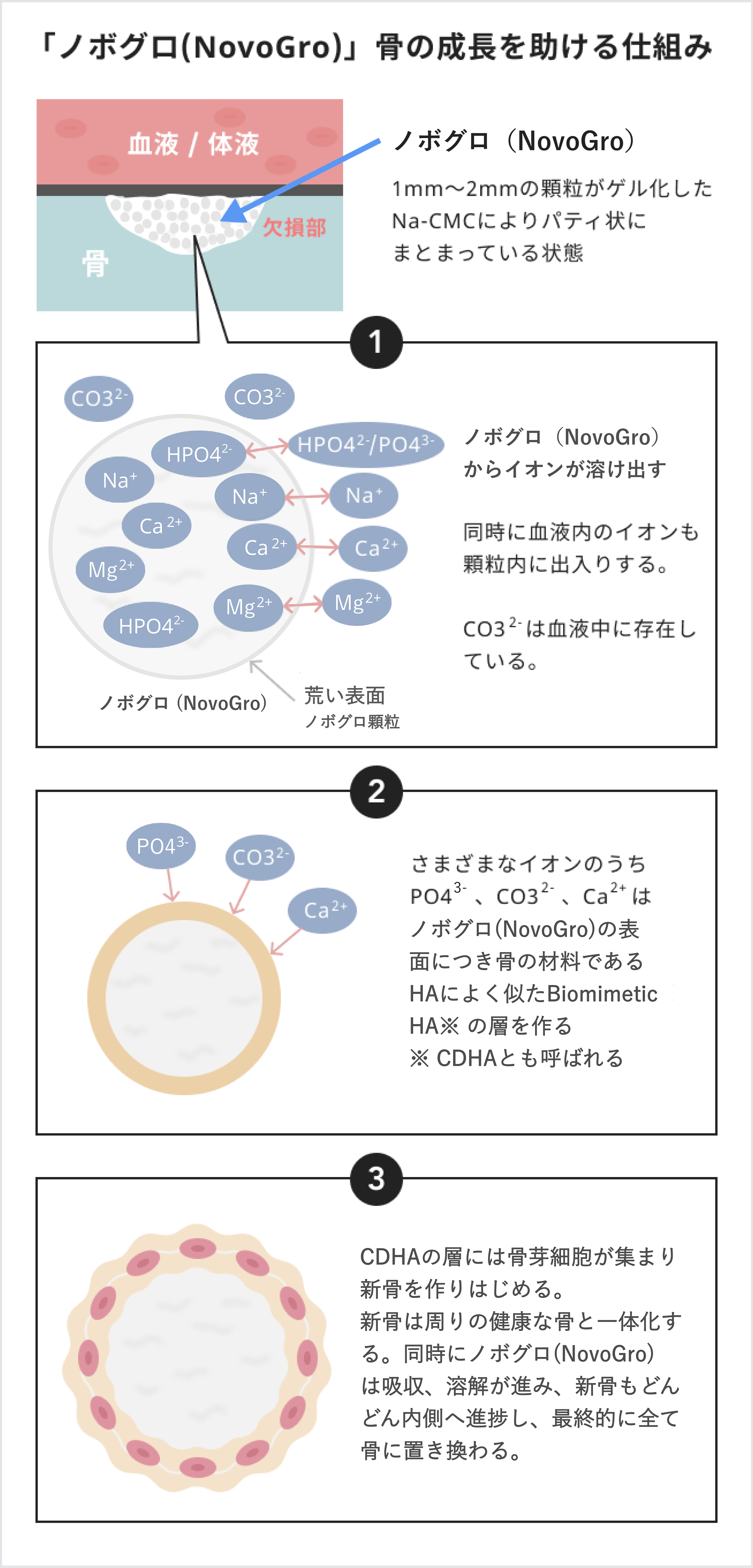
「ノボグロ (NovoGro)」はまず無機材料を調整し一旦顆粒を作り、最終的に手術室で水と混ぜ合わせ、パティ状 (粘土状) にします。調整した材料個々の成分は安全性が確認されています。生物由来(人の骨や動物性コラーゲン等) の原料も全く使用しておらず、とても安全です。しかも粘土のように骨の形状に合わせて貼り付けられるなど、手術時に使いやすいように設計されています。
「ノボグロ (NovoGro)」の特徴は材料の組み合わせにもあります。考案したOsteoNovus Inc.創業者の1人であるバドゥーリ(Bhaduri)教授は特許を取得しており、弊社独自の配合です。一般的な人工骨の素材はβ-TCPやハイドロキシアパタイトといったリン酸カルシウムを主体に構成されますが、「ノボグロ (NovoGro)」はリン酸カルシウム以外に、リン酸マグネシウム、リン酸ナトリウム、酸化マグネシウム等を組み合わせています。これら様々な材料で構成することにより、体内に移植した際にCa2+、Mg2+、Na+といった様々なイオンが溶けだし、骨芽細胞を募り、骨再生を助けます。

「ノボグロ(NovoGro)」ではさらにシリカを加え、粗面を形成し、より細胞がつきやすい構造にしました。また、顆粒の表面に加えたカルメロースナトリウム粉末は、水と混ざるとゲル状になり顆粒同士を結合させ、最終的にパティ状になります。1つ1つの材料は全て日本国内で既に医薬品や食品として使用されており、安全性が確認されたもの。カルメロースナトリウムも、動物性のコラーゲンを使用していないため感染症等のリスクも無く、安心して手術に使用していただけると確信しています。
オステオノバス株式会社は米国OsteoNovus Inc.の100%子会社として2020年1月に設立されました。日本法人の役割は日本を含むアジア太平洋地区での事業開発です。中国を除くと、日本は最大にして最重要市場。まずPMDA(独立法人医薬品医療機器等総合機構・厚労省所管)の審査を経て厚労省の承認を取得し製品の販売を開始します。
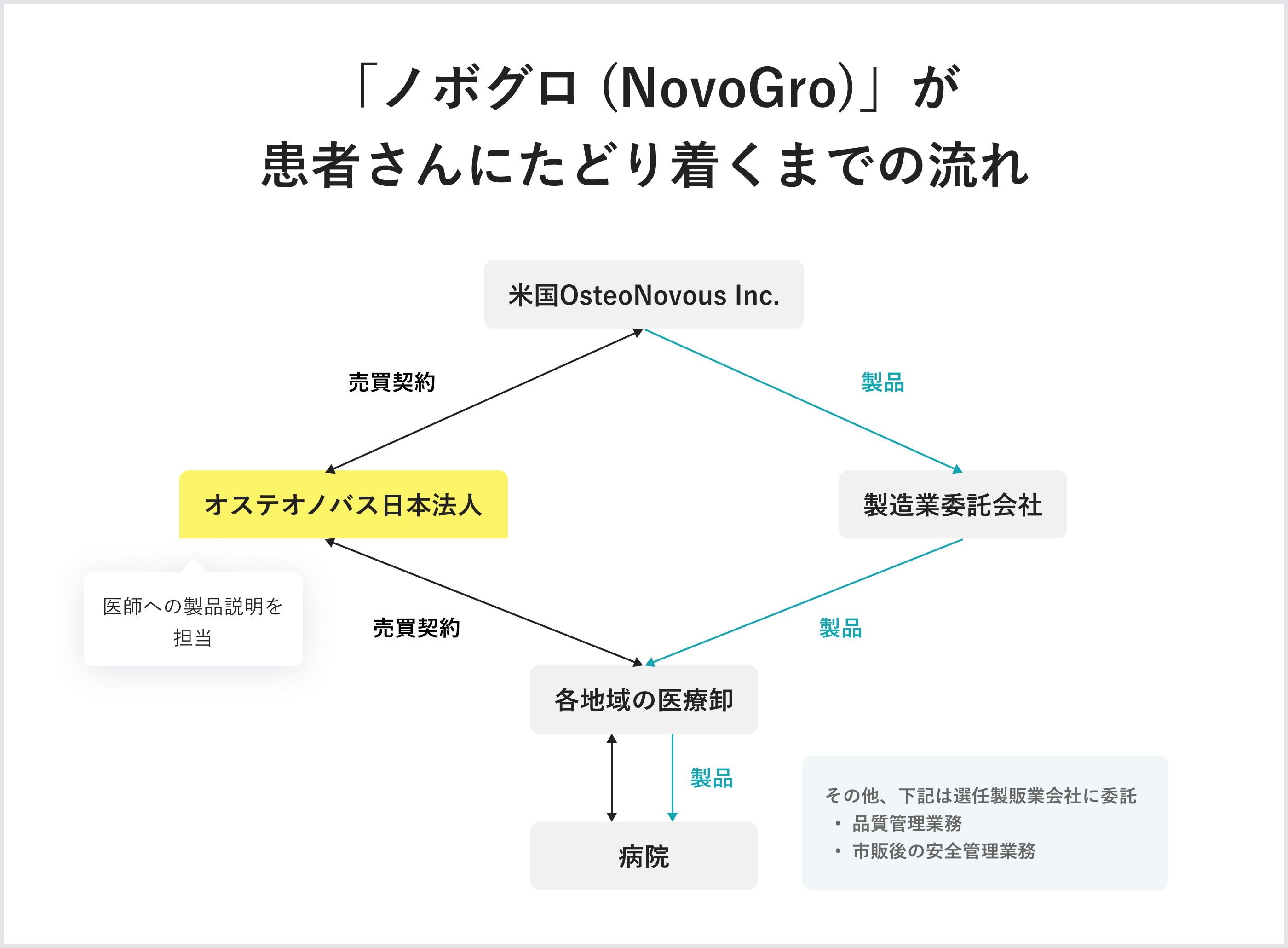
米国オハイオ州にある工場で生産した「ノボグロ(NovoGro)」を日本に空輸し、国内の流通システムで各医療機関にお届けします。米国にある製造施設はISO13485※をクリアしており、材料の生産からパッケージングまで行います。医師への説明は当社が直接行います。販売・配達は医療機器業界では一般的なモデルで、医療卸さん経由となります。
※ISO13485は、医療機器産業に特化した品質マネジメントシステムに関する国際規格。日本を含む世界各国の医療機器に関する規制において、品質管理手法のベースとして採用されています。
並行して台湾食品医薬品局(TFDA)に対する承認申請を行い、本年6月9日(水)に無事取得できました。これから製品登録の手続きにはいります。台湾については総代理店を起用し同社に販売を任せます。台湾の次は豪州進出を検討しています。
また、事業がある程度成長し販売額が5億円を越え10億円が視野に入る段階で、日本に製造拠点を設ける考えです。製造原価低減、アジア市場向けパッケージの開発、デリバリータイムの短縮効果・在庫管理の容易さなどを考慮の上最終判断していきます。
人工骨は脊椎外科や整形外科手術で使用されます。対象となる手術は脊柱管狭窄症や脊柱変形などの治療のために施される脊椎固定術、骨腫瘍切除、股関節再置換術などで、日本国内における脊椎固定術は年間約7万件行われています。また、膝・股関節の関節再置換術で年間約4千件行われています。他にも骨腫瘍切除術や、偽関節の手術等にも人工骨は使用されていて、全ての手術を合わせると10万件ほど行われていると推測します。市場規模で表すと約100億円の規模となります。親会社が直接担当している米国の骨再生材料市場は約600億円。アジアその他の地域の市場についてはデータ不十分でマーケットの推定は困難なものの、アジア太平洋市場は中国を含めると人口規模で日本の20倍。人口増加と高齢化の加速で、アジア太平洋の骨再生材料市場は成長が期待される市場であると考えています。

日本においては、脊椎外科の専門医がおられる病院は全国で約千施設。人工関節置換術をある程度頻繁に行っている施設もほぼ同数あります。その中で主要な約500施設程度をターゲットにします。
日本で人工骨自社製品(OEM製品含む)を販売している会社は、脊椎外科手術関連製品全般を扱っている米国の大手メーカー群と、人工骨を中心に製品を構成している日本メーカー数社があります。
使い勝手と安全性を考慮すると、吸収性骨再生材料の「ノボグロ (NovoGro)」の製品力は非常に優れています。また米国市場に比べ、類似製品が非常に少ないため高シェアを狙えると判断しています。
初年度は基礎固めの年です。アドバイザーの先生方のネットワークを中心に、症例検討や臨床研究を行い「ノボグロ (NovoGro)」が実際に臨床上有用であるという実績を積みます。エビデンスをベースに学会で発表して頂いたり、セミナーを開催。そうした活動を通して専門医の先生方の認知度を高めます。(Pull Strategy)
2年目以降は活動の幅を拡げます。地域の有力代理店さんや、脊椎外科領域に強いメーカーさんで人工骨をお持ちでないところと組み、B2Bのアプローチを展開します。タイアップを通じて全国を面で捉えられるような動きをしていきます。
当社の強みは製品力と先生方とのユニークなネットワーク。日本の脊椎外科手術をリードする先生方をアドバイザーにお迎えし、先生方のネットワークを構築します。当社の創業者の1人であるDr. Vijay Goel教授は脊椎・整形外科領域のバイオエンジニアリングの大家です。多くの日本の脊椎外科の先生方が同教授をご存知で、「ノボグロ (NovoGro)」の優れた特徴を早い段階でご理解頂けると考えています。
一方で弱みは営業力と製品の品揃えです。当社の営業員は少数精鋭のため、大手メーカーさんの数百人の営業部隊には量的に対抗できません。脊椎外科手術では数多くの製品を利用されます。当社は人工骨専業ですので、大手メーカーさんの品揃えにはかないません。しかしこれは競合する部分が小さいので、補完的なアライアンスを組むチャンスが大きいとも言えます。

強みを十分生かし、弱みについては、B2Bの仕組みを作ることでもう一つの成長エンジンにしたいと思います。
売上規模としては3年目で7億円、5年目で10億円強を目指します。
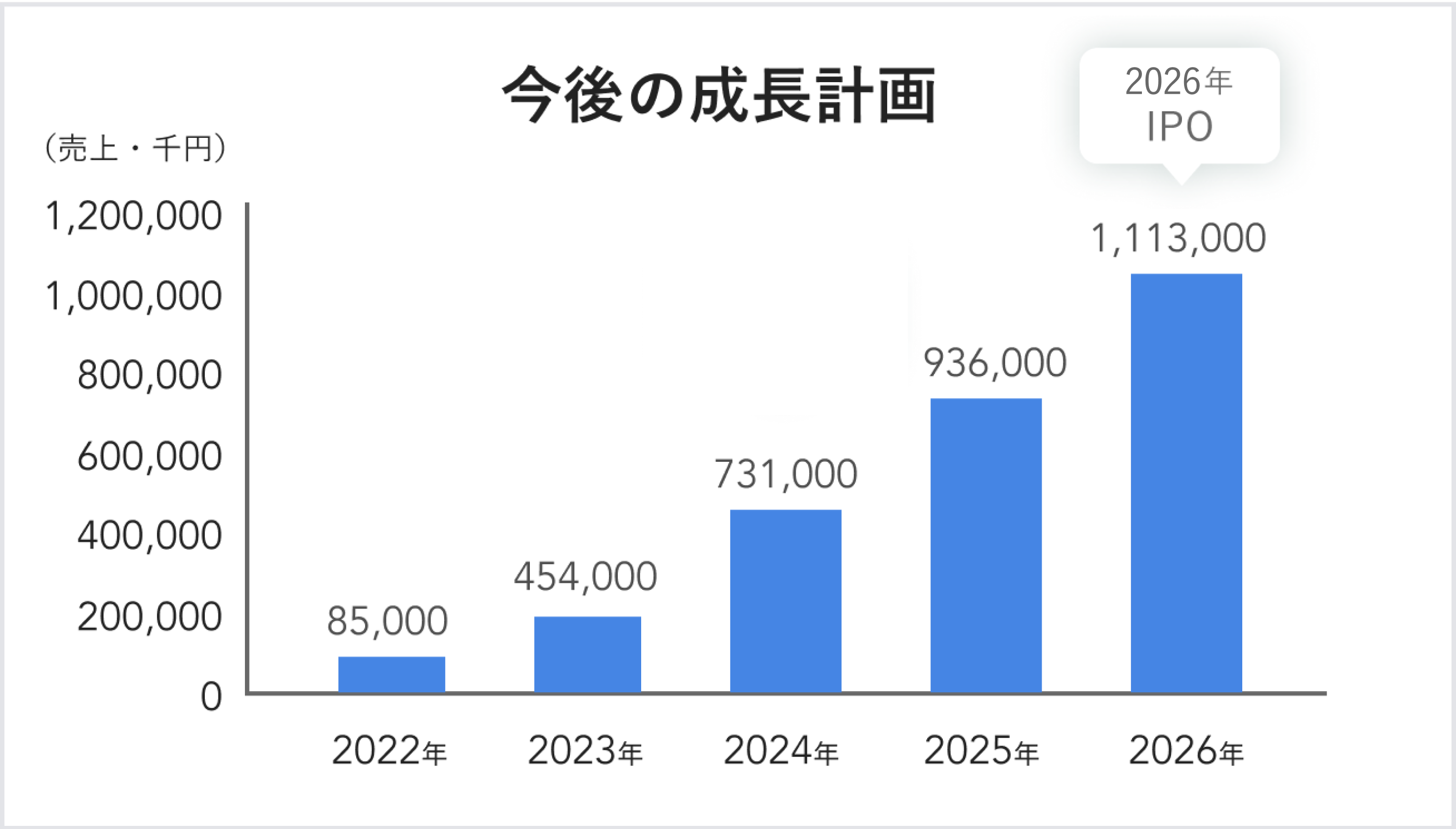
当社は米国法人の子会社ですが、日本市場での評価が高まれば、親会社を子会社化したうえで日本で上場することを視野に入れています。日本国内では競合する製品選択肢がとても少ないため、ある程度シェアを獲得できれば日本での事業評価が米国での評価より高くなる可能性があります。その場合米国で上場するよりも日本で上場する選択肢が現実味を帯びます。
今回調達させて頂く資金は、PMDAの審査を経て厚生労働省の承認を取得するまでの運転資金として活用させて頂きます。主に非臨床試験費用、PMDA申請関連費用、人件費などに使用します。これまで会社として7,000万円程度調達しています。仮に3,000万円を調達させて頂けると丁度1億円程度になり、承認取得までの費用を賄える計画です。
数値計画の詳細につきましては、こちらの書面をご覧ください。
新株発行概要書
代表取締役社長
森 崇
丸紅(10年半)GE(15年)キヤノン(7年半)三菱ケミカル(2年)と勤務。後半の17年間ヘルスケア事業の経営や製品開発リーダーを歴任(放射性医薬品事業、画像診断機器開発、化学を生かす医療事業開発)。キャリア前半では事業開発、営業・マーケ、M&A、PMI、サービス体制再構築を担った。2019年秋OsteoNovus Inc.のVPに就任し2020年1月当社設立。大阪大学基礎工学部物性物理工学科卒、UCLA経営大学院卒(MBA)趣味:美術館・博物館巡り、いろんな野球を観る事(元高校球児)、ホームパーティ

代表取締役会長(非常勤)
Anand Agarwal, MD
CEO, OsteoNovus Inc.脊椎外科医として独・英で臨床医を18年務めた。2011年トレド大学教授。2013年同大学教授2名とOsteoNovus Inc.を創業。外科医のかたわら医療機器開発に関わり医療機器メーカー数社のアドバイザーを15年以上務めた。国際学会を多数企画し日本の脊椎外科医にも知己が多い。保有特許約100件。論文・学会発表多数。Bundelkhand Univ. (Medical College)卒。趣味:スポーツカーとF1(独サーキットチームの救急医を務めたほど)、旅行、写真

アソシエイト
西良 恵理子
会社設立と同時に入社。PMDA申請書作成や非臨床試験モニターを担当。社内人事制度設計にも携わった。承認取得後はプロダクトスペシャリストとして専門医へのコミュニケーションを担う予定。University of Toledo(USA)卒Biology専攻。趣味:美味しいお酒とご飯、歌うこと、いろんな楽器、外国語(スペイン語)

技術アドバイザー
榊 敏朗
(現)田辺三菱製薬に入社以来一貫して医療・医薬品分野で研究開発・新規事業立ち上げを企画推進した。人工骨マーケティングの経験を持つ。2015年よりフューチャーデザイン/デジタルトランスフォーメーション部門専門部長として医療の未来を切り開く新規領域を担当。また2020年に新規技術および事業のリーンスタートアップをコーチングするSAT研究所を設立し所長に就任。当社では技術面を中心にアドバイスを提供している。東京大学大学院理学系研究科卒(薬学博士)。趣味:ワイン、ストリートダンス、海外旅行

オペレーションアドバイザー
太田 祐司
某自動車部品メーカーにて将来のユーザー体験から求められるコックピットの企画開発やシステム開発に従事している。前職のキヤノン㈱では眼科機器の光学設計・画像設計を統括した。また一時事業企画部門へ異動し中期製品ポートフォリオの設計とプロモーション施策を立案した。当社においてはPSIコントロールを始め業務ワークフローの設計をアドバイス予定。大阪大学大学院工学研究科卒。趣味:美味しい珈琲を豆から淹れる、ぬか漬けを漬ける、旅行、BBQ、ウォーキング
推薦の言葉
整形外科医にとって、骨折から人工関節、脊椎の手術に至るまで、骨と骨をつなぎ合わせることは整形外科手術の基礎であり、骨欠損を補う骨補填材料(骨再生材料・人工骨)の良し悪しは手術における生命線の一つであります。
従って、骨補填材料のイノベーションは、整形外科手術を大きく進化させてきました。
古くは骨欠損部を埋めるだけのガラスビーズから始まり、現在ではβ―TCPや脱灰ヒト皮質骨などの補填材そのものが骨に置き換わる材料に進化しています。
「ノボグロ(NovoGro)」は現在までに使用された骨補填材料のどれとも異なる性質を持ちます。ペースト状の「ノボグロ(NovoGro)」は様々な形に変化し、骨欠損部の隅々まで充填することができます。
また、ビーズとパテから構成される「ノボグロ(NovoGro)」独自の構造は、挿入直後から患部の安定を得ることができ、早期からの離床や退院に役立ちます。
さらに「ノボグロ(NovoGro)」は、人骨を加工した脱灰ヒト皮質骨と違い、100%合成であるため、プリオン病を含む未知の感染症に罹患する可能性を完全に否定します。
良い骨補填材料は手術技術を大幅に改良します。「ノボグロ(NovoGro)」は間違いなく、革新的な骨補填材料であり、私は整形外科医として「ノボグロ(NovoGro)」の未来を約束します。

沿革
2013年 OsteoNovus Inc. 設立(米国オハイオ州)
2014年 Ohio Innovation Fund (TVSF)獲得
2015年 製造所設立(米国オハイオ州)
2017年 ISO13485取得、NovoGro Putty FDA510K取得(整形領域)
2018年 NovoGro Putty FDA510K取得(脊椎領域)、The R&D100 受賞(発明界のオスカーアワード)
2020年1月 オステオノバス㈱設立
2021年6月 非臨床試験(安全性)完了
2021年8月 PMDA承認申請予定

5株 100,000円単位
払込金額の総額(上限募集額を発行の場合)4,200万円のうち、発行諸費用として約845万円を差し引いた後の手取概算額3,355万円については、PMDA申請費用(400万円)、人件費(2,300万円/年)及び安全性及び有効性検証のための非臨床試験費用(655万円)に充当します。払込金額の総額が、1,000万円(目標募集額を発行の場合)以上4,190万円以下であった場合、発行諸費用を除く手取概算額(746万円~3,346万円)については、前記同様に、PMDA申請費用や人件費、安全性及び有効性検証のための非臨床試験費用に充当します。募集金額に応じてPMDA申請費用・人件費へ優先的に充当します。
なお、事業計画は、目標募集額による調達を前提に作成しており、目標募集額を超える調達が行われた場合は、2022年7月末までに予定している第2回株式投資型クラウドファンディングによる公募又は第三者割当増資及び融資により調達する金額を調整する予定です。
自社による株主名簿管理となります。
以下において、発行会社の事業及び業績に重要な影響を及ぼす可能性がある事項を記載しております。また、必ずしもそのようなリスク要因に該当しない事項につきましても、重要であると考えられる事項につきましては、積極的な情報開示の観点から以下に示しております。発行会社は、これらのリスク発生の可能性を十分に認識した上で、リスクの軽減策を講じるとともに、発生した場合の対応に努める方針としていますが、本項の記載事項をご精読いただき、十分にご理解いただきたくお願い申し上げます。
以下において、発行会社の事業及び業績に重要な影響を及ぼす可能性がある事項を記載しております。
以下において、発行会社の事業及び業績に重要な影響を及ぼす可能性がある事項を記載しております。また、必ずしもそのようなリスク要因に該当しない事項につきましても、重要であると考えられる事項につきましては、積極的な情報開示の観点から以下に示しております。発行会社は、これらのリスク発生の可能性を十分に認識した上で、リスクの軽減策を講じるとともに、発生した場合の対応に努める方針としていますが、本項の記載事項をご精読いただき、十分にご理解いただきたくお願い申し上げます。
以下において、発行会社の事業及び業績に重要な影響を及ぼす可能性がある事項を記載しております。